Esta proporciona información de la sustancia objeto de estudio.
NATURALEZA ELECTROMAGNÉTICA DE LA LUZ
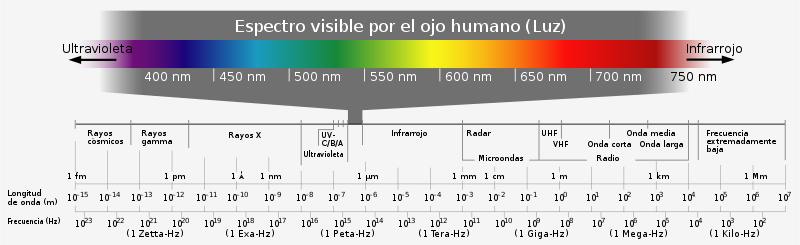
Además del espectro de luz visible por el ojo humano hay tipos de luces más allá del especrto visible por el ser humano (clasificados por la frecuencia de la onda electromagnética), las cuales son:
-ELF(Extemely low frequency)
-VLF(Very low frequency)
-Radio
-Microondas
-Infrarrojos
-Ultravioleta
-Rayos X
-Rayos gamma
ESPECTROSCOPIA ATÓMICA
Un átomo aislado en fase gaseosa puede emitir y absorber radiación electromagnética.
Cuando un átomo es excitado con un a fuente de energía externa como podría ser la térmica, emiten luz. Al descomponer y analizar la luz emitida se obtiene un espectro de emisión atómica.
Por lo contrario, si se ilumina un átomo aislado y se analiza el espectro de luz que lo atraviesa se obtiene un espectro de absorción atómica.
La posición y la anchura de las líneas de luz que se analizan en el espectro obtenido son como una huella dactilar del elemento químico.

ESPECTROSCOPIA IR
La técnica de la espectroscopia IR (infrarroja) es la más empleada para la identificación molecular.
Cuando los átomos de una molécula se excitan vibran. La luz infrarroja tiene la frecuencia y energía ideales para provocar estas vibraciones moleculares.
Cada enlace tiene una frecuencia característica de vibración, por lo que si iluminamos un compuesto con luz ultravioleta, cada enlace de esta absorberá su frecuencia característica dando lugar a un espectro de absorción IR.
ESPECTROMETRÍA DE MASAS
Al contrario de otras técnicas espectrométricas, la espectrometría de masas no está basada en la interacción de la luz con la materia. En este proceso no se obtiene un espectro de radiaciones electromagnéticas, sino que se obtienen fragmentos de materia.
Esta técnica es más precisa que las demás y su principal aplicación es la determinación de masa atómicas/moleculares.
Esta técnica funciona de la siguiente manera:
Información sacada de "Física y Química 1º Bachillerato ANAYA"

























